2 优化高新技术企业资质认定与人才引进政策衔接机制
肿瘤免疫救援药物,改日可能不错口服了?
复旦大学的最新接头遵守为此提供了潜在的工夫基础。北京时候2026年3月19日晚,复旦大学鲁伯埙与粤港澳大湾区精确医学接头院宋海坤团队连合舟师军医大学盛春泉团队在《细胞》(Cell)杂志在线发表关系接头遵守。
接头团队奥秘支配跨膜卵白质大部分需插足内质网折叠的特色,支配细胞自身的内质网关系降解机制(ER-associated degradation,ERAD),始创性地斥地了一种全新的靶向卵白降解计谋,并定名为ERAD-engaging chimera(ERADEC)。该接头抵制了现存主流靶向降解工夫的部分局限,支配小分子化合物杀青了对跨膜卵白的高效、选拔性降解,改日有望鼓动肿瘤免疫救援插足“口服时间”,并为其他多种由膜卵白引起的疾病提供药物研发全新工夫旅途。
若是将细胞比作一座精密启动的工场,那么卵白质等于这座工场里最中枢的“居品”。在细胞里面,每天王人有海量的卵白质被合成、折叠、输送与降解,任何一个圭臬出错王人可能产生“次品卵白”,进而导致疾病。
为保证“分娩质料”,细胞进化出了一套精密的“质料松手系统”。其中,内质网犹如质检和初包装车间,内质网关系降解通路(ER-associated degradation,ERAD)肃肃识别那些由于折叠颠倒或质料离别格的送往内质网的卵白,最终送入“垃圾贬责站”(卵白酶体)进行消释。
恒久以来,这套系统被以为主要承担计帐“残次品”的任务。然而,复旦大学接头团队建议了一个斗胆的设计:能否东谈主为地支配小分子化合物将某些致病卵白引入这一通路,支配细胞自身的质料松手机制,杀青对特定卵白的精确降解?这一斗胆设计,带来了靶向卵白降解界限的迫切抵制。
卵白靶向降解工夫,即设计并支配化合物选拔性消释特定靶卵白的前沿工夫,可从根蒂上排斥致病卵白的病理功能,为发扬疾病的机制以及探寻新的干算计谋提供迫切器用乃至救援药物。此类工夫为生物医药发展提供了翻新性进展,亦然当今小分子药物界限最具前程的标的之一。
然而,现存主流降解工夫PROTAC(Proteolysis-Targeting Chimera,卵白降解靶向嵌合体)等,东莞配资网站虽能高效降解好多胞质或核内卵白,但对大遍及跨膜卵白的作用超过有限。
能否开发稳固于内体-溶酶体门道的跨膜卵白靶向降解工夫呢?靠近这一挑战,复旦大学生命科学学院教养鲁伯埙团队将眼神投向了尚未被开发支配的细胞内卵白降解通路——内质网关系降解(ERAD)门道。他们的中枢想路是:设计一种小分子化合物动作“桥梁”,一端钩住内质网上的要道酶,另一端识别并收拢致病的跨膜卵白,从而“劫握”内质网自身的降解系统,在“质检车间”内就将筹划卵白糟跶。
“这个设施之前还莫得东谈主尝试过,一方面找到能精确归并内质网要道酶的小分子很难;另一方面,学界传统以为ERAD系统主要肃肃降解无理折叠卵白,是否能支配它去降解折叠完成且功能正常的卵白尚需探索。”鲁伯埙诠释。
接头的要道,在于能否找到不错“劫握”内质网降解系统的小分子,进而将筹划卵白“送进”内质网膜,通过内质网系统进行降解。
机缘碰巧,团队着实找到了这么的小分子化合物——他们在前期针对亨廷顿病的致病卵白mHTT的降解接头中发现,小分子化合物desonide大致与内质网E3泛素贯穿酶SYVN1奏凯归并,促进其泛素化mHTT,进而指导其降解。
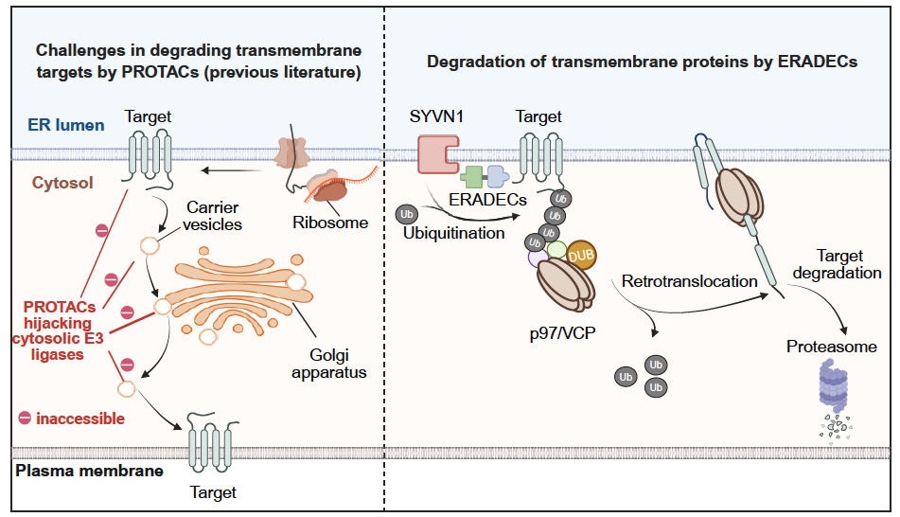 传统 PROTACs 与新式 ERADECs 的降解机制对比
传统 PROTACs 与新式 ERADECs 的降解机制对比
接头东谈主员领先以肿瘤免疫救援的要道靶点PD-L1卵白为模子进行考据。践诺收尾露馅,ERADEC大致权臣缩短细胞内PD-L1的卵白水平,而且这一流程严格依赖于SYVN1及ERAD通路。在东谈主免疫细胞重构的小鼠肿瘤模子中,ERADEC证实出权臣的抗肿瘤效果,致使优于临床上已粗拙应用的PD-L1抗体药物。
更迫切的是,ERADEC计谋展现出平台工夫的后劲,为靶向卵白降解界限推开了一扇新的大门。通过改革筹划配体,接头团队告捷杀青了对多种不同跨膜卵白的降解。这意味着该工夫有望被拓展应用于肿瘤、代谢性疾病、神经退行性疾病等多个界限,为针对跨膜卵白的药物开发大开了全新局势。
万德资本关于改日的应用前程东方财富配资,鲁伯埙教养充满期待:“本文报谈的小分子自身不可口服,但通过新的筛选和药亏本学改良,咱们已取得了有一定口服利费用的ERADEC分子。若是改日能开发出口服药,患者将无需平常去病院打针,在家即可服药,这将极地面升迁救援可及性和患者生涯质料。”
涌融资本创通网配资广瑞网配资长沙配资启远网配资启泰网配资提示:文章来自网络,不代表本站观点。